Definición del problema
En esta sección se explicará la complejidad y el alcance del problema. Se expandirá sobretodo desde la perspectiva médica dado que es el tema del que las autoras saben menos al enfrentarse con este problema.
Desde la perspectiva médica
Hay muchos elementos a partir de los cuales se puede clasificar a los tumores cerebrales. Como punto de partida, los tumores cerebrales pueden nacer en el cerebro, denominados tumores cerebrales primarios. O si el cáncer se disemina al cerebro desde otra parte del cuerpo, estos tumores son tumores cerebrales secundarios, y también se conocen como metastásicos. En este trabajo nos centraremos en los tumores primarios, y dentro de ellos, los gliomas. Esta última clasificación surge del tipo de células que conforman al tumor, en la Figure 1 se puede ver esta clasificación. Los tumores cerebrales pueden crecer a partir de los nervios (neurinoma), la duramadre (meningioma) o la glándula pituitaria (craneofaringioma o adenoma pituitario). También pueden crecer a partir del propio tejido cerebral (glioma). A medida que crecen, pueden comprimir el tejido normal y causar síntomas. Dentro de todos estos tipos de tumores existen unos 120 tipos más específicos, por lo que solo nos explayaremos respecto al relevante para este trabajo 12.
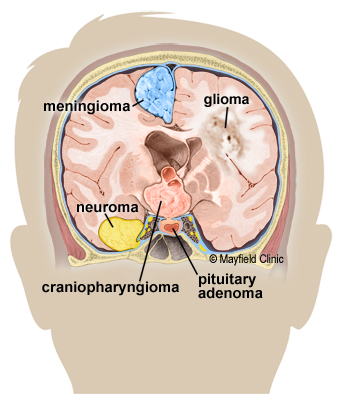
Glioma es un tipo común de tumor que se origina en el cerebro, aunque a veces puede encontrarse en la médula espinal 3. Alrededor del 33% de todos los tumores cerebrales son gliomas. Estos tumores surgen de las células gliales que rodean y brindan soporte a las neuronas. Existen varios tipos de células gliales, por lo tanto, hay muchos tipos de gliomas, incluyendo Astrocitomas, Oligodendrogliomas y Ependimomas, los cuales forman parte del desafío de este proyecto.
La comprensión de los gliomas ha ido evolucionando con los años. Dependiendo del tipo de células que forman el glioma y sus mutaciones genéticas, estos tumores pueden ser más o menos agresivos. Según la OMS 4, existen los siguientes grados de tumores primarios del sistema nervioso central:
| Grado | Descripción |
|---|---|
| Grado I | Tumores circunscritos, de lento crecimiento y bajo potencial de conversión a un tumor de mayor malignidad. |
| Grado II | Tumores de borde difuso, lento crecimiento y, algunos, con tendencia a progresar a tumores de mayor malignidad. |
| Grado III | Tumores infiltrantes con células atípicas o anaplásicas y mayor número de mitosis. |
| Grado IV | Tumores de rápido crecimiento con alta tasa mitótica, pudiendo presentar vasos de neoformación y áreas de necrosis. |
Si bien el tamaño del tumor no es un indicador inmediato de su grado (y menos aún del del cáncer, pues son grados diferentes), el ritmo de crecimiento del mismo y la definición de los bordes sí lo es. Esto aumenta la dificultad en la segmentación de tumores malignos, dado que sus bordes suelen ser muy difusos. Además, los tumores cerebrales suelen acumular fluido (llamado edema) a su alrededor, así como hinchazón en la zona afectada. Esto también puede dificultar la detección, y es importante definir el problema a resolver, es decir, si la detección es solo del tumor, o del tumor con edema, o de ambos por separado.
En general, los tumores suelen identificarse utilizando resonancia magnética, dado que es un método no invasivo y tiene resolución suficiente para identificar y medir ciertas propiedades de los tumores. En este contexto, no es una tarea difícil para un especialista identificar la presencia de un tumor (razón por la cual la clasificación no es tan atractiva) pero sí su ubicación precisa y su tamaño. Esto es esencial para planear el tratamiento del mismo: influirá sobre la decisión de si se puede remover por cirugía o no; la dosis y área de radioterapia 5. En todo caso, para hacer una estimación del volumen/tamaño observando solo las imágenes siempre es necesario estimar una de las dimensiones. El especialista puede delinear el área del tumor en una de las imágenes y a partir de una estimación de la profundidad se puede estimar el volumen; para hacer un cálculo más preciso debería tomarse todas las distintas profundidades de MRI, delinearlas todas y multiplicar cada una de las áreas por su grosor correspondiente, un trabajo muy exhaustivo. De hecho, es como se generan las etiquetas de segmentación en la mayoría de los casos. De aquí es que surge el gran beneficio de poder hacer una segmentación volumétrica del tumor utilizando directamente su representación en 3D.
Finalmente, se hará un breve hincapié en los tipos de resonancia magnética que se utilizan en general para resolver este problema, y los pasos de preprocesamiento que se necesitan. Una de las características principales de la resonancia magnética es el tiempo de relajación 6:
-
T1 (Tiempo de Relajación Longitudinal): Es el tiempo que tarda el vector de magnetización en recuperarse en un 63% de su valor original después de haber sido perturbado por un pulso de radiofrecuencia. En imágenes ponderadas en T1, los tejidos con tiempos de relajación T1 más cortos (como la grasa) aparecen brillantes, mientras que los tejidos con tiempos de relajación T1 más largos (como el líquido cerebroespinal) se ven oscuros. Las imágenes ponderadas en T1 son útiles para visualizar la anatomía y detectar anomalías estructurales como tumores.
-
T2 (Tiempo de Relajación Transversal): Es el tiempo que tarda el vector de magnetización en decaer al 37% de su valor máximo después de ser perturbado. En imágenes ponderadas en T2, los tejidos con tiempos de relajación T2 más largos (como el líquido cerebroespinal) aparecen brillantes, mientras que los tejidos con tiempos de relajación T2 más cortos (como la grasa) se ven oscuros. Las imágenes ponderadas en T2 son útiles para identificar patologías, ya que muchas lesiones tienden a tener un mayor contenido de agua y, por lo tanto, un tiempo de relajación T2 más largo.
Además, se utilizan diferentes pasos de preprocesamiento de resonancia magnética, incluyendo el registrado de imágenes, la corrección del campo de sesgo, y la eliminación de tejido no cerebral.
Desde la perspectiva de computer vision
La segmentación es un proceso fundamental que implica dividir una imagen en partes o regiones significativas, facilitando su análisis e interpretación. La segmentación puede abordar varios problemas específicos, como la detección de bordes y la detección de regiones.
-
Detección de Bordes: Consiste en identificar los límites o contornos de los objetos dentro de una imagen. Esto es crucial para reconocer la forma y el tamaño de los objetos. Los algoritmos de detección de bordes buscan cambios abruptos en la intensidad de los píxeles, que normalmente indican la presencia de un borde.
-
Detección de Regiones: Se enfoca en agrupar píxeles que comparten características similares, como color, textura o intensidad, formando regiones coherentes. Esto ayuda a identificar y aislar objetos completos dentro de la imagen, facilitando tareas como el etiquetado y la clasificación de objetos.
Cualquiera de los dos caminos puede resultar en la segmentación de una zona de interés, y los métodos sobre los que se desarrollará a continuación son alguna variación de estos dos tipos.
La definición generaliza a volúmenes en 3D, hablando de contornos como superficies y regiones como volúmenes. Además, las medidas de performance usuales en imágenes (como el IoU) no contemplan toda la variabilidad que tienen las soluciones en 3D, por lo que se presentarán dos nuevas de las que no se suele hablar en imágenes 2D, que son relevantes en este estudio. Dos de las más comunes son la distancia de Hausdorff y el coeficiente de Dice.
| Métrica | Definición | Relevancia |
|---|---|---|
| Dist. de Hausdorff | Mide el grado de similitud entre dos conjuntos de puntos, considerando la mayor de todas las distancias mínimas desde un punto en un conjunto hasta el punto más cercano en el otro conjunto. | Es útil para evaluar la precisión de la segmentación en términos de la localización de los bordes. Una menor distancia de Hausdorff indica que los bordes segmentados están más cerca de los bordes reales del objeto. |
| Coeficiente de Dice | El coeficiente de Dice es una medida de similitud que evalúa la superposición entre dos conjuntos de datos. Se calcula como el doble del volumen de superposición dividido por la suma de los volúmenes de los dos conjuntos. | Es una métrica muy utilizada para evaluar la precisión de la segmentación de regiones. Un valor de Dice más alto indica una mayor superposición entre la segmentación predicha y la verdad del terreno, lo que sugiere una segmentación más precisa y efectiva. |
Por último, un tema relevante a través de todos los modelos de estado del arte presentados son los modelos difusos (fuzzy models) 7, por lo que parece relevante presentar qué son de manera general en esta sección. Son modelos matemáticos que utilizan lógica difusa (no binaria) para manejar y representar la incertidumbre y la imprecisión en datos y conocimiento. Son particularmente relevantes en el contexto de la segmentación de imágenes médicas, debido a varias fuentes de imprecisión inherentes a este tipo de datos:
- Imprecisiones en las imágenes: los límites de los tumores suelen ser imprecisos debido a la naturaleza del fenómeno observado, es difícil definir de por sí dónde empieza y termina el tumor. Además, el sistema de adquisición y el proceso de reconstrucción numérica pueden introducir imprecisiones espaciales e intensidad.
- Conocimiento disponible: El conocimiento sobre los niveles de grises de los tejidos cerebrales principales está sujeto a imprecisiones. Aunque se conoce el orden constante de los niveles de grises, el rango exacto de valores para cada tejido es impreciso.
-
Mayfield Clinic. Brain tumors: an introduction. 2018. URL: https://mayfieldclinic.com/pe-braintumor.htm. ↩
-
Mayo Clinic. Tumor cerebral. 2023. URL: https://www.mayoclinic.org/es/diseases-conditions/brain-tumor/symptoms-causes/syc-20350084. ↩
-
Johns Hopkins Medicine. Brain tumor types. 2024. URL: https://www.hopkinsmedicine.org/health/conditions-and-diseases/brain-tumor/brain-tumor-types. ↩
-
Mariana Sinning. Clasificación de los tumores cerebrales. Revista Médica Clínica Las Condes, 28(3):339–342, 2017. Tema central: Tumores cerebrales. URL: https://www.sciencedirect.com/science/article/pii/S0716864017300597, doi:https://doi.org/10.1016/j.rmclc.2017.05.002. ↩
-
PhD Jorg Dietrich, MD. Clinical presentation, diagnosis, and initial surgical management of high-grade gliomas. April 09 2024. Literature review current through: Jun 2024. URL: https://www.uptodate.com/contents/clinical-presentation-diagnosis-and-initial-surgical-management-of-high-grade-gliomas. ↩
-
Daisuke Kawahara and Yasushi Nagata. T1-weighted and t2-weighted mri image synthesis with convolutional generative adversarial networks. Reports of Practical Oncology and Radiotherapy, 26(1):35–42, 2021. URL: https://doi.org/10.5603/RPOR.a2021.0005, doi:10.5603/RPOR.a2021.0005. ↩
-
Hassan Khotanlou, Olivier Colliot, Jamal Atif, and Isabelle Bloch. 3d brain tumor segmentation in mri using fuzzy classification, symmetry analysis and spatially constrained deformable models. Fuzzy Sets and Systems, 160(10):1457–1473, 2009. Special Issue: Fuzzy Sets in Interdisciplinary Perception and Intelligence. URL: https://www.sciencedirect.com/science/article/pii/S0165011408005368, doi:https://doi.org/10.1016/j.fss.2008.11.016. ↩